截至6月30日,FDA已經批準了16款創新藥,其中包括9款化藥新藥和7款生物藥新藥,First-in-class藥物占據半壁江山(8款)。
從適應癥上看,腫瘤藥物獲批最多,一共有7款,免疫領域有3款,其他領域各1款。與此同時,罕見病領域研發依舊火熱,一共有4款藥物上市。
值得一提的是,今年上半年的新藥獲批數量明顯少于去年,2024年同期已有21款新藥獲批,主要是化藥新藥上市數量減少(去年同期有14款化藥新藥上市),這一現象反映了FDA審批標準的嚴格性在持續強化。
表1 2025年上半年,FDA批準新藥盤點
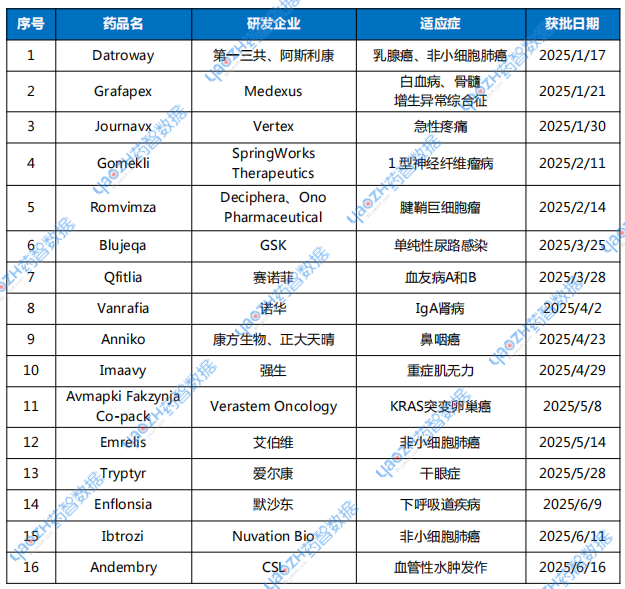
數據來源:藥智數據、FDA官網
腫瘤領域:ADC爆發、靶向治療再升級
2025年上半年,ADC在腫瘤治療領域迎來新突破。兩款關鍵ADC的獲批填補了實體瘤靶向治療的空白,而首款KRAS突變卵巢癌療法的問世則標志著協同抑制策略的成熟,共同推動腫瘤領域精準治療進入新階段。
Datroway:乳腺癌與肺癌的雙重突破
阿斯利康與第一三共聯合開發的Datroway成為上半年焦點。該藥物由人源化的、靶向在乳腺癌和肺癌中高表達的Trop-2的單克隆抗體與DNA拓撲異構酶I抑制劑(DXd))連接。搭載的拓撲異構酶I抑制劑DXd,活性比傳統化療藥伊立替康高10倍,且具備強膜滲透性,可觸發“旁觀者效應”,在殺傷靶細胞后擴散至鄰近腫瘤細胞,克服腫瘤異質性難題。
Datroway于2025年1月獲得FDA批準,用于治療既往接受過內分泌治療和化療的HR陽性、HER2陰性不可切除或轉移性乳腺癌成人患者,并在6月獲得FDA加速批準治療NSCLC。
Emrelis:攻克肺癌難治亞型
艾伯維的Emrelis于5月獲批,聚焦c-Met高表達非鱗狀NSCLC,該亞型預后極差且缺乏靶向方案,通過抗體靶向c-Met受體,釋放微管蛋白抑制劑MMAE直接破壞癌細胞分裂,是首個批準用于治療c-Met過度表達的經治療晚期NSCLC的療法。
Avmapki Fakzynja Co-pack:KRAS耐藥困境的破局者
Verastem Oncology的Avmapki Fakzynja Co-pack由Avutometinib和Defactinib組成。其中Avutometinib是具有口服活性的MEK1抑制劑,Defactinib是FAK和Pyk2的抑制劑。FAK/RAF/MEK抑制可協同誘導黑色素瘤細胞體外凋亡,促進體內腫瘤消退,延長已有腦轉移瘤小鼠的存活時間。該藥物于5月8日獲FDA批準,用于治療復發性低級別漿液性卵巢癌(LGSOC)成年患者,這些患者曾接受過系統性治療并且其腫瘤攜帶KRAS突變。
罕見病邁向“精準治療”時代
長久以來,罕見病治療常囿于“藥物匱乏”的困境,傳統療法往往僅能緩解癥狀或效果有限。然而,2025年上半年獲批的4款創新療法,正推動罕見病治療領域邁入“精準治療”新時代。
Andembry:預防遺傳性血管性水腫發作的首款因子XIIa靶向療法
Andembry是一種抗FXIIa的單克隆抗體,特異性抑制血漿蛋白FXIIa。當FXII被激活時,會啟動導致水腫形成的級聯反應。通過靶向FXIIa,Andembry能在反應最初階段就阻斷級聯反應的信號傳導。該藥于6月16日獲得FDA上市,用于預防成人和12歲及以上兒童患者遺傳性血管性水腫(HAE)發作,它是首款只需每月一針、靶向血漿蛋白因子XIIa(FXIIa)的HAE發作預防療法。
Qfitlia:可治療所有血友病類型的siRNA療法
3月28日,FDA批準賽諾菲和Alnylam聯合開發的siRNA療法Qfitlia上市,用于預防或減少12歲以上血友病A和血友病B患者的出血事件。Qfitlia通過降低抗凝血酶水平,從而促進凝血酶生成,重新平衡止血功能并預防出血。由于這一獨特作用機制,它可以治療多種不同類型的血友病,大大擴展了它的應用范圍。在兩項3期臨床試驗中,它只需每月一次皮下注射,就可將患者的年化出血率降低90%。在有些患者中,給藥次數可降低到每兩個月一次。
Gomekli:潛在“best-in-class”別構小分子抑制劑
Gomekli是一種口服別構小分子MEK抑制劑,靶向MEK1和MEK2。2月11日,FDA批準Gomekli上市,用于治療年齡不低于2歲的1型神經纖維瘤病相關叢狀神經纖維瘤(NF1-PN)成人和兒童患者。它是首個獲批可同時用于治療成人和兒童NF1-PN的藥物,有望成為兒童NF1-PN患者的“best-in-class”療法。此外,FDA還授予了該藥物快速通道資格,用于治療2歲及以上的神經纖維瘤病1型相關的叢狀神經纖維瘤患者。它的新藥申請也曾獲得FDA授予的優先審評資格。
Rommviva抗腫瘤口服小分子療法
Rommviva是一種口服酪氨酸激酶抑制劑,專門設計用于選擇性和強效抑制CSF1R,有效抑制CSF1R的自磷酸化及下游信號傳導,從而抑制腫瘤細胞的增殖和存活。該藥品由Deciphera Pharmaceuticals開發,2024年4月Ono Pharmaceutical與Deciphera達成并購協議,斥資24億美元收購了Deciphera公司并囊獲這款療法。2025年2月14日,美國FDA批準Romvimza(vimseltinib)上市,用于治療腱鞘巨細胞瘤(TGCT)患者。
關于舉辦四川省藥品生產企業擬新任質量
各相關企業: 新修訂的《中華人..四川省醫藥保化品質量管理協會召開第七
四川省醫藥保化品質量管理協會第七..“兩新聯萬家,黨建助振興”甘孜行活動
為深入貫徹落實省委兩新工委、省市..學習傳達中央八項規定精神專題會議
2025年4月22日,協會黨支部組織召..關于收取2025年度會費的通知
各會員單位: 在過去的一年里,..學習八項規定 增強警示教育
近日,四川省醫藥保化品質量管理協..《持續合規 提質創新》 2025年度四川省
2025年3月24至3月27日,四川省醫藥..四川省應對新型冠狀病毒肺炎疫情應急指
四川省應對新型冠狀病毒肺炎疫情應..四川省應對新型冠狀病毒肺炎疫情應急指
四川省應對新型冠狀病毒肺炎疫情應..